Herstellung zellulärer Produkte

Ihr CDMO-Partner für Zell- und Gentherapieprodukte
Cellex ist einzigartig! Als Full-Service-Anbieter bieten wir umfassende Expertise in allen Bereichen der Zelltherapie-Herstellung – von der Bereitstellung des zellulären Starting Material bis zur Herstellung und Lieferung der fertigen Zelltherapie-Produkte. Wir können Sie von der präklinischen Entwicklung über die klinische Herstellung bis hin zur Vermarktung unterstützen.
Warum Cellex für die Herstellung von Zell- und Gentherapien wählen?
Fachwissen:
Wir verfügen über mehr als 10 Jahre Erfahrung in der Herstellung und Prüfung von Zwischen- und Endprodukten in der Zell- und Gentherapie.
Produktionskapazität und Flexibilität:
Die Produktionsanlagen von Cellex bieten erhebliche Kapazitäten. Wir verfügen über ein hohes Maß an Fachwissen bei der Ausstattung von Reinräumen nach Kundenspezifikationen. Zudem können die Reinräume individuell gestaltet werden.
Produktqualität:
Wir verfügen über ein breites Portfolio an Analysetechnologien, die in hochmodernen Qualitätskontrolllabors angewendet werden. Unter Berücksichtigung aller bestehenden Gesetze und Richtlinien können wir eine kontrollierte, gesetzeskonforme und gleichbleibend hochwertige Produktion gewährleisten.
Zeitplan:
Als Full-Service-Anbieter mit Expertise in allen Bereichen unterstützen wir Sie dabei, Produkte so schnell wie möglich zu entwickeln und einen reibungslosen Ablauf zu gewährleisten. Ein engagierter Programmmanager entwickelt einen Projekt- und Zeitplan und stimmt diesen mit Ihnen ab.
Prozessentwicklung und -optimierung:
Wir können Sie vom Technologietransfer Ihres Forschungsprodukts über die Prozessoptimierung bis hin zur kommerziellen Produktion Ihrer ATMPs/CGTs unterstützen. Sie können auch von unserer Erfahrung in der kommerziellen Prozessoptimierung profitieren, die zu erheblichen Kosteneinsparungen führen kann.
QP-Dienstleistungen:
Die Chargenzertifizierung wird von einem Team sehr erfahrener qualifizierter Personen (QPs) durchgeführt.
Logistik:
Cellex bietet maßgeschneiderte und GDP-konforme Transportmöglichkeiten. Die geografische Lage der Produktionsstätten mitten in Mitteleuropa sichert logistische Vorteile durch etablierte Transportnetzwerke.
Geschulte Mitarbeitende:
Intensive Schulungen im hauseigenen Schulungszentrum garantieren, dass unsere spezialisierten und erfahrenen Mitarbeitende immer auf dem neuesten Stand sind.
Projektmanagement über den gesamten Projektzyklus:
Hochqualifizierte und erfahrene Projekt-Managerinnen und Projekt-Manager unterstützen die Entwicklung, Implementierung, Optimierung und Qualifizierung von Prozessen.

Von der Strategie bis zur Markteinführung
Komplexer Entwicklungs- und Produktionsprozess für zellbasierte Therapeutika
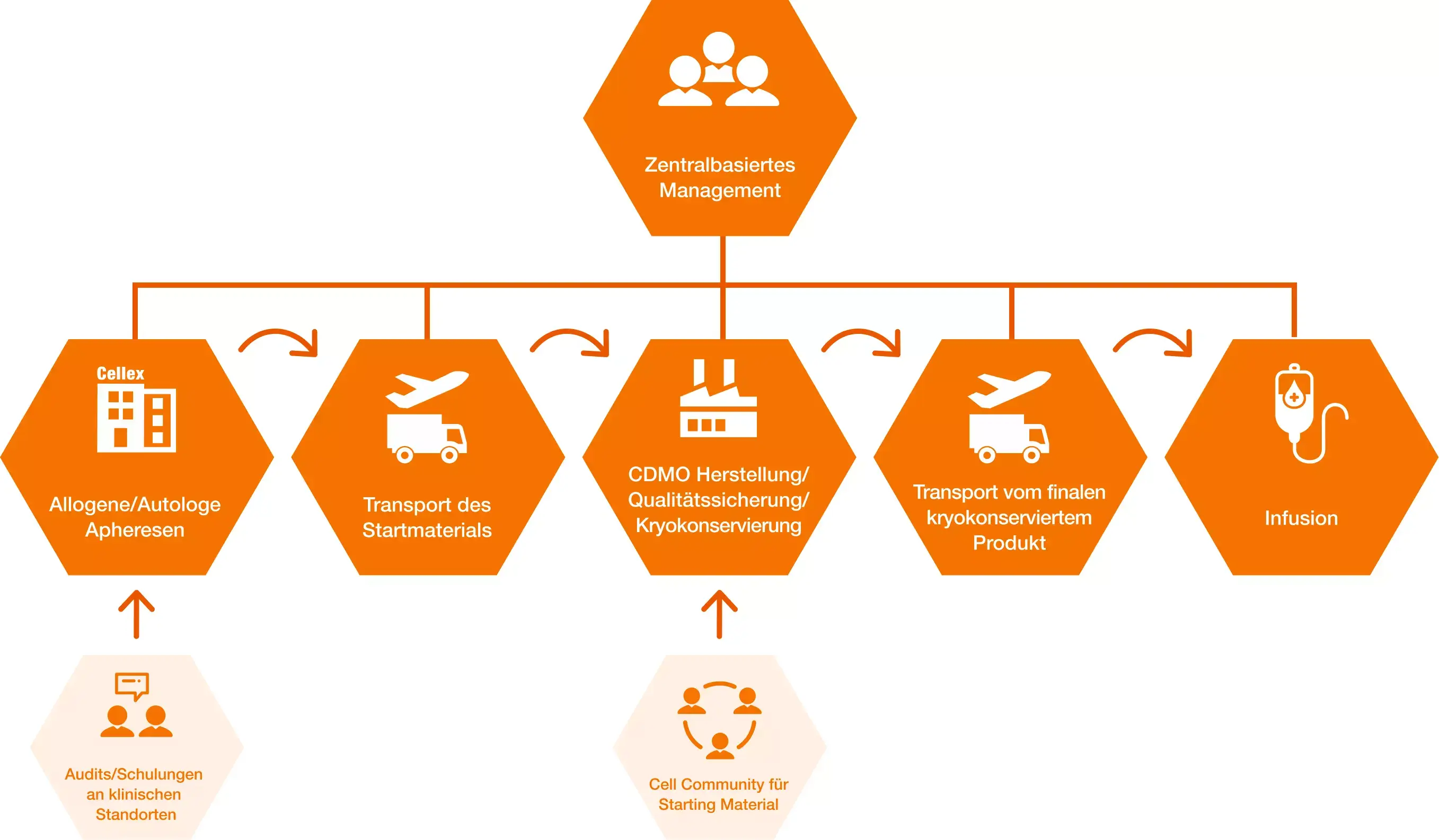
In unserer modernen Cellex Cell Manufacturing Plant (CCMP) stellen wir sowohl innovative zelluläre Zwischenprodukte (ITM) als auch fertige Arzneimittelprodukte her und unterstützen damit unsere Kunden in ihrem Ziel, Patientinnen und Patienten, die an einer Vielzahl von Krankheiten leiden, den Zugang zu neuen Therapien zu ermöglichen. Die Produktion erfolgt auf der Basis von allogenem oder autologem Zellmaterial und wird gemäß den Kundenspezifikationen und GMP-Richtlinien durchgeführt.
Unsere hochqualifizierten Mitarbeitenden unterstützen Sie mit ihrer Expertise bei der individuellen Prozessentwicklung. Mit der Herstellungslizenz in der Hand können die Produkte in klinischen Studien und für kommerzielle Zwecke eingesetzt werden. Wenn Sie bereits über einen definierten Herstellungsprozess verfügen, führen wir einen Technologietransfer durch und kümmern uns um die Prozessentwicklung bis zur großtechnischen Herstellung.
Derzeit Herstellung von 4 FDPs (Endprodukte) und 7 zellulären Zwischenprodukten

> 2,500 m2 GMP zugelassene Produktionsstätte mit Reinraumsuiten und Ballsälen

Über 5.800+ produzierte Chargen – 100% der vom Sponsor angeforderten Chargen wurden erfolgreich hergestellt

Herstellung von CGT/ATMP-Produkten
Die GMP-konforme Anlage verfügt über modernste Reinräume der Klassen C und D mit individuell anpassbaren und ausgestatteten Produktionssuiten. Im Laufe der Jahre haben wir große Erfahrung darin gesammelt, bereits bestehende Herstellungsprozesse durch steriles Andocken in ein geschlossenes System zu überführen. Sind offene Prozessschritte (Klasse A ISO/5 Containment) erforderlich, so werden diese in einem Isolator durchgeführt.
Die folgenden Standardprozessschritte sind etabliert und werden für mehrere Kunden verwendet:
- Selektion oder Verarmung spezifischer Zellpopulationen
- Genetische Modifikation von Zellen, z. B. mit viralen Vektoren oder CRISPR/Cas9-Technologie
- Expansion
- Füllen und Veredeln
- Kryokonservierung
- Nehmen Sie Kontakt mit uns auf, um zu besprechen, wie wir Sie bei der Herstellung von ATMPs/CGT-Produkten unterstützen können und wie Sie von unserer Erfahrung profitieren können.
Qualitätsmanagement
Cellex arbeitet mit einem pharmazeutischen Qualitätssystem, um die Einhaltung aller relevanten Gesetze und Vorschriften zu gewährleisten, einschließlich
- EudraLex Band 4, insbesondere Teil IV, Anhang 1, 11, 13, 14, 15, 16, 19
- ICH Q2, Q5C, Q6B, Q7, Q8, Q9 und Q10
- Leitlinie zu Qualität, nicht-klinischen und klinischen Aspekten von Arzneimitteln, die genetisch veränderte Zellen enthalten (CAT/CHMP/GTWP/671639/2008)
- Leitlinie über zellbasierte Humanarzneimittel (EMEA/CHMP/410869/2006)
- Leitlinie zur Wirksamkeitsprüfung von zellbasierten Immuntherapeutika für die Behandlung von Krebs (EMEA/CHMP/BWP/271475/2006)
Unser Team sorgt dafür, dass relevante Prozesse wie Änderungskontrolle, Korrektur- und Vorbeugungsmaßnahmen (CAPA) und Abweichungsmanagement reibungslos ablaufen.
Der gesamte Produktionsprozess wird von den ersten Qualifizierungsschritten der Geräte und Verfahren bis zur Freigabe des Produkts überwacht. Die zugehörigen Dokumente wie SOPs, Qualifizierungs- und Validierungsprotokolle, Material- und Lieferantenqualifizierung usw. werden von den Mitarbeitenden des Qualitätsmanagements erstellt und gepflegt. Unser Qualitätsmanagementsystem (QMS) wird ständig überwacht und aktualisiert, um die Einhaltung der gesetzlichen Vorschriften sowie der höchsten Qualitäts- und Sicherheitsstandards zu gewährleisten.
Wenn Sie Audits durchführen möchten, ist dies nach vorheriger Absprache möglich.
Qualitätskontrolle
Die Qualitätskontrolle mit einem breiten Spektrum an Methoden wird intern oder in externen Vertragslabors mit validierten Methoden durchgeführt.
Sichtprüfung/Visual Inspection
- Durchflusszytometrie (Analyse verschiedener Zellpopulationen durch Bestimmung von Größe, Granularität und Antigenexpression auf der Zelloberfläche mittels fluoreszenzmarkierter Antikörper)
- Blutbildanalyse (automatisierte Analyse der Blutbestandteile)
- Sterilitätsbestimmung, Testung auf Endotoxin und Mycoplasmen
- Potency Assay zur quantitativen Messung der biologischen Aktivität
- Impendanzmessung und bildgebende Zytometrie zur Zellzahlbestimmung
- Bildgebende Zytometrie (Vitalitätsbestimmung)
Automatisierte und schnelle Analyse der Blutbestandteile
Unsere Mitarbeiterinnen und Mitarbeiter verfügen zudem über umfassende Expertise im Bereich der Kryokonservierung und beraten Sie zum Transport der Produkte.
Lesen Sie hier weiter.
QP-Freigabe
Ein erfahrenes Team von Sachkundige Personen (QP, Qualified Persons) ist für die Einhaltung der einschlägigen pharmazeutischen Vorschriften verantwortlich, prüft und kontrolliert alle relevanten Daten und Unterlagen und zertifiziert das Produkt anhand eines IMPD oder einer Marktzulassung.